Base de données des minéraux luminescents
DIAMANT (Nom en anglais: DIAMOND )
Formule chimique: C
Famille: Eléments
Statut: IMA-GP
Système cristallin : Cubique
Minéral de vitrine: OUI
Luminescence:
Couleurs UV longs (365nm): |
Bleu , Blanc bleuté , Blanc jaunâtre (crème) , Blanc rosâtre , Jaune pâle , Jaune , Orange brunâtre , Rouge , Rose saumon (rose orange) , Jaune vert , Vert , Bleu , Blanc verdâtre , Jaunâtre , | ||
Intensité OL:Forte | Fréquence OL:Souvent | ||
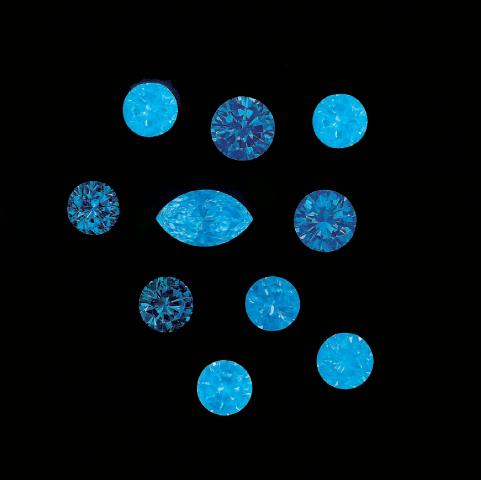
Photo en lumière du jour

Diamant, Congo;
Photo et col. G. Barmarin
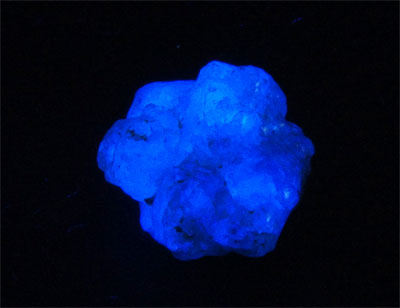
Photo Ondes longues (365nm)

Diamant UVLW (superbright 2000), Congo;
Photo et col. G. Barmarin
Galerie de photos:


 ...
...  Accès à la galerie complète (21 images au total)
Accès à la galerie complète (21 images au total)
Vous avez une photo de ce minéral que vous voudriez voir figurer dans la galerie? Contactez-nous!
Phosphorescence (au sens commun du terme) observable à l'oeil nu:
Type d'UV |
Couleur |
Intensité |
Fréquence d'observation |
|---|---|---|---|
UV longs (365nm): | Blanc bleuté | Forte | Souvent | UV courts (254 nm): | Rouge | Forte | Très rarement |
Triboluminescence: OUI
Thermoluminescence: OUI
Commentaires:
Probablement le minéral le plus anciennement connu pour sa phosphorescence après exposition au soleil. Robert Boyle signale déjà en 1663 la triboluminescence du diamant quand on le broie. Une triboluminescence bleue ou rouge est parfois observée lorsque l'on scie les diamants avant de les tailler. L'épouse du célèbre minéralogiste Kunz possédait un diamant prodigieux qui était phosphorescent pendant plusieurs minutes après avoir été simplement exposé à la lumière d'une petite lampe de poche électrique. En 1895, Kunz a attribué la fluorescence et la phosphorescence de certains diamants à la présence d'un hydrocarbure hypothétique, qu'il a nommé tiffanyite . On peut estimer en moyenne à un sur quatre le nombre de diamants naturels fluorescents. Les diamants bleus naturels sont des semi-conducteurs et émettent de la lumière quand ils sont traversés par un courant électrique (électroluminescence)
Activateur(s) et spectre(s):
Activateur(s): N (Azote), B (Bore),
Pics dans le spectre (nm):
N3 center: 442, 507 nm
H3 center: 520nm
A-band center: 452nm
N3 center: 415, 428, 439, 452, 731nm

Galerie de spectres:
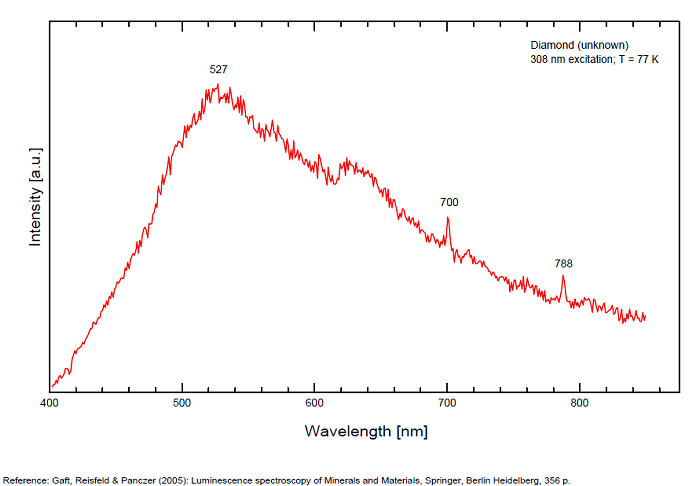
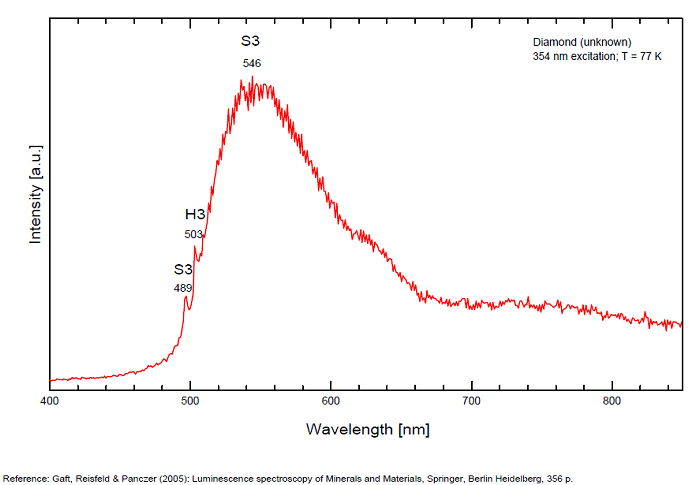
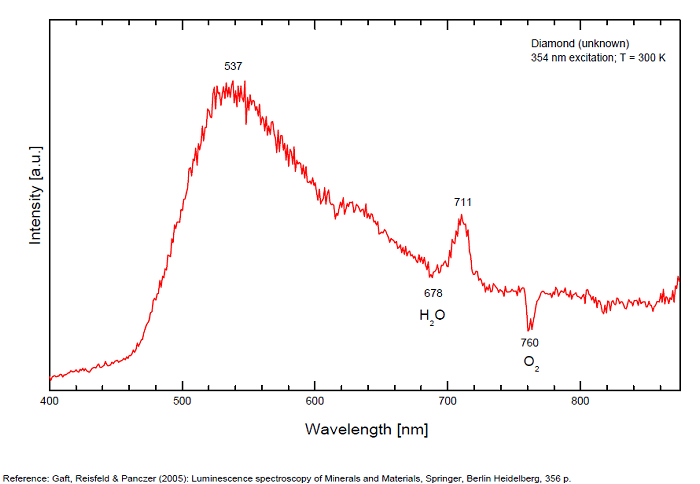
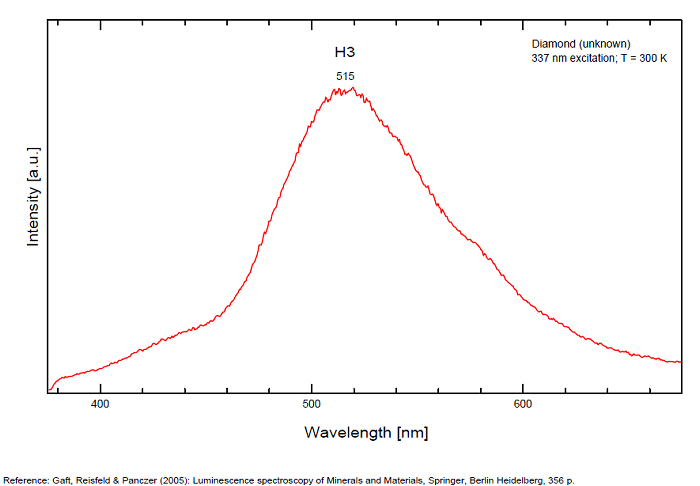 ...
...  Accès à la galerie complète (13 images au total)
Accès à la galerie complète (13 images au total)
Commentaires sur les spectres et les activateurs (*):
From more than 100 detected centers only for seven the models are determined, mainly based on EPR interpretations. The model includes identification of the impurity, vacancy, interstitial atom, their aggregations and their crystallochemical position together with quantum-chemical and spectroscopic description. (Gaft) Luminescence of diamond is related to various defects in its structure, almost always related to N (Nitrogen) atoms. It is logical, because the atomic radii of C and N are nearly equal (approximately 0.77 Å). N3 center: color and luminescence center attributed to 3 Nitrogen atoms bounded to the same Carbon atom or a vacancy. The luminescence spectra of this center is associated with a large peak at 440-450nm with a fine structure (peaks around 415, 428, 438 and 451nm) a lifetime: 30-40ns and an absoption energy of 2,985eV but other centers (Al imputity for exemple) contribute to this spectrum even if it is not possible aboce 170K to discriminate their contribution. H3 and H4 centers: 496, 506, 512nm ; two Nitrogen atoms coupled with a vacancy in two different configurations. Absorption energy: 2,463eV. Decay-time: 15-20ns S1 center: a combination of one vacancy with one Nitrogen atom, 541nm S2 center: a combination of two vacancies with one Nitrogen atom, 565nm S3 center: a combination one vacancy with several Nitrogen atom H3, H4, S2 and S3 centers are characterized by broad bands at 520-545nm with very weak lines at 489nm and 523nm (S2), 498nm (S3) and 503nm (H3) A-band at 480nm observed in natural diamond of type I A-band with a maximum at 440 nm in natural diamond of type II (low Nitrogen diamonds) Some blue diamonds exhibit a remarkable red phosphorescence such as Hope or Wittelsbach-Graff (both of Indian origin) and Blue Moon (South Africa Cullinan Mine); All natural, untreated type IIb blue diamonds (diamond without Nitrogen but containing some uncompensated Boron) show a phosphorescence with two emission bands: one at 660 nm and another at 500 nm but for those three diamonds, unlike usually, it is the blue that decreases more quickly than the red causing this magnificent red phosphorescence. Type IIb diamonds with orange-red phosphorescence are more commonly originated in India or Venezuela but not in the case of the blue Moon coming from the Cullinan Mine in South Africa where diamond are normally found with a more typical brief bluish phosphorescence. After exposure to short-wave ultraviolet light, the Blue Moon display orange-red phosphorescence (around 660nm) that remain visible for up to 20 seconds. (see bibliography: Eloise Gaillou, Gems and Gemmology, Winter 2014)
(*)Les commentaires sur les spectres sont uniquement rédigés en Anglais
Meilleure(s) localité(s) pour la fluorescence (*):
- Mbuji Mayi, Kasaï-Oriental, DR Congo
(*)Les données ne sont pas exhaustives et sont limitées à quelques localités remarquables pour la fluorescence
Référence bibliographique pour la luminescence:
- The Henkel Glossary of Fluorescent Minerals, Dr. Gerhard Henkel, Published by the FMS, 1989 ,
- Fluorescence: Gems and Minerals Under Ultraviolet Light, Manuel Robbins, 1994, Geoscience Press, ISBN 0-945005-13-X ,
- The World of Fluorescent Minerals, Stuart Schneider, Schiffer Publishing, 2006, ISBN 0-7643-2544-2 ,
- Luminescence Spectroscopy of Minerals and Materials, M. Gaft, R. Reisfeld, G. Panczer, Springer Editor, ISBN: 10 3-540-21918-8 ,
- Luminescent Spectra of Minerals, Boris S. Gorobets and Alexandre A. Rogojine, Moscow, 2002 ,
- Handbook of Fluorescent Gems and Minerals, a practical guide for the gem and mineral collector, Jack de Ment, 1949 ,
Référence pour la luminescence sur internet:
- Luminescence/phosphorescence of the "Blue Moon" Diamond, Eloise Gaillou, Gems and Gemmology, Winter 2014;
- A Gemological Study of a Collection of Chameleon Diamonds, Thomas Hainschwang, Dusan Simic, Emmanuel Fritsch, Branko Deljanin, Sharrie Woodring, and Nicholas DelRe, GIA
Videos:
- https://www.youtube.com/watch?v=l81qETV_5xQ
- The phosphorescing diamond: https://www.youtube.com/watch?v=Hu3Xs7Fj_u8
- How does fluorescence affect the look of a diamond? https://www.youtube.com/watch?v=XY5_neHP5aU
Référence minéralogique sur internet:
 http://www.mindat.org/show.php?name=Diamond
http://www.mindat.org/show.php?name=Diamond
 http://webmineral.com/data/Diamond.shtml
http://webmineral.com/data/Diamond.shtml
Recherche sur Internet:
 Recherche d'images sur 'Google Image'
Recherche d'images sur 'Google Image'
 Recherche de documents en français sur Google
Recherche de documents en français sur Google
 Recherche de documents en toutes
langues sur Google
Recherche de documents en toutes
langues sur Google
Une requête ne donnant pas de résultat signifie uniquement qu'aucune référence de ce type n'existe dans la base mais en aucun cas qu'elle n'existe pas dans l'absolu. Si vous considérez avoir trouvé une erreur ou une omission, merci de nous le signaler via la page contact en n'oubliant pas de citer la source de l'information.